Miembro de la familia
Smad tipo 6 |
|---|
| Estructuras disponibles |
|---|
| PDB | Buscar ortólogos: PDBe, RCSB |
|---|
| Identificadores |
|---|
| Símbolos | SMAD6 (HGNC: 6772) ; AOVD2; HsT17432; MADH6; MADH7 |
|---|
Identificadores
externos | - OMIM: 602931
- MGI: 1336883
- HomoloGene: 4079
- EBI: SMAD6
- GeneCards: Gen SMAD6
- UniProt: SMAD6
|
|---|
| Locus | Cr. 15 q22.31 |
|---|
| | | Función molecular | • promotor de la ARN polimerasa II, región proximal del ADN
• unión a cromatina
• factor de transcripción: secuencia específica de unión a ADN
• unión proteica
• mediador de inhibición citoplasmática del receptor del factor de crecimiento transformante-beta
• unión a proteína ligasa de ubiquitinas
• unión al receptor del factor de crecimiento transformante-beta tipo 1
• unión multi-proteica
• unión a región regulatoria de la transcripción en el ADN
• unión a iones metálicos
• unión a co-SMAD
• unión a I-SMAD
• unión a R-SMAD
• unión al receptor tipo 1 de la activina
|
|---|
| Componente celular | • núcleo
• complejo del factor de transcripción
• citoplasma
• citosol
• complejo proteico
|
|---|
| Proceso biológico | • desarrollo del muñón embrionario de la uretra
• transcripción moldes en el ADN
• respuesta inmune
• vía de señalización del receptor del factor de crecimiento transformante-beta
• especificación del eje axial y ventral en el cigoto
• regulación negativa de la proliferación celular
• regulación negativa del ensamblaje del complejo SMAD
• vía de señalización BMP
• regulación negativa de la vía de señalización del receptor del factor de crecimiento transformante-beta
• regulación negativa de la vía de señalización BMP
• adhesión célula a sustrato
• respuesta al estrés hidrodinámico
• transducción de señales intracelulares
• regulación negativa del proceso de apoptosis
• respuesta al estrógeno
• diferenciación de células adiposas
• regulación negativa de la vía de fosforilación de la vía Smad
|
|---|
| Referencias: AmiGO / QuickGO | |
|---|
| Patrón de expresión de ARNm |
|---|
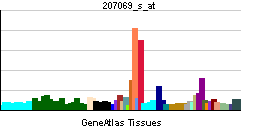 |
 |
| Más información |
| Ortólogos |
|---|
| Especies | |
|---|
| Entrez | |
|---|
| Ensembl | |
|---|
| UniProt | |
|---|
RefSeq
(ARNm) | |
|---|
RefSeq
(proteína) NCBI | |
|---|
| Ubicación (UCSC) | Cr. 15:
66.7 – 66.78 Mb | Cr. 9:
63.95 – 64.02 Mb | |
|---|
| PubMed (Búsqueda) | |
|---|
|
[editar datos en Wikidata] |
SMAD6 (por su siglas en inglés Mothers Against Decantaplegic homolog, donde "Decapentaplegic" se refiere a una proteína descubierta en moscas que es Homóloga a la proteína morfogénica ósea humana), es uno de nueve miembros de la familia Smad, una proteína que, en los humanos, es codificado por el gen SMAD9.[1]
Nomenclatura
Smad2 pertenece a la familia de proteínas SMAD implicadas como moduladores de la expresión de genes pertenecientes a múltiples vías de señalización celular.[2] El nombre Smad deriva de la contracción del nombre de dos proteínas, la primera inicialmente identificada en la Drosophila melanogaster (MAD o «Mothers against decantaplegic» y la expresión «mothers against» adicionada como un apunte de humor a la anécdota anglosajona que las madres usualmente forman organizaciones de protesta) y la segunda es una proteína del nemátodo Caenorhabditis elegans (SMA o «small body size», que corresponde a genes mutados que alteran el tamaño corporal). Combinando las dos siglas Sma + Mad se obtine el de la proteína en cuestión: Smad, que es notoriamente homóloga a las anteriores.[3]
Función
Como es el caso con otras proteínas Smad, Smad6 sirve de mediadora en la vía de señalización del factor de crecimiento transformante-beta (TGF-beta)[4][5] y para señales propias de la proteína morfogénica ósea.[6] Sus actividades son inhibitorias y actúan en oposición al Smad4 en una gama de actividades biológicas que incluyen el crecimiento celular, la apoptosis y la diferenciación celular.[7]
Interacciones
La proteína Smad6 ha demostrado ser capaz de interaccionar con:
- HOXC8,[8]
- MAP3K7,[9][10]
- Smad7,[11]
- PIAS4, y[12]
- STRAP.[13]
Referencias
- ↑ «Entrez Gene: SMAD6 SMAD family member 6».
- ↑ Wrana JL, Attisano L (2000). «The Smad pathway». Cytokine Growth Factor Rev. 11 (1–2): 5-13. PMID 10708948. doi:10.1016/S1359-6101(99)00024-6.
- ↑ Vanegas, Adriana Lucía, & Vásquez, Gloria María. (2011). Smad y otros blancos terapéuticos en esclerodermiaSmad and other therapeutic targets in scleroderma Revista Colombiana de Reumatología, 18(4), 285-294. Accesado el 18 de diciembre de 2015
- ↑ Verschueren K, Huylebroeck D (2000). «Remarkable versatility of Smad proteins in the nucleus of transforming growth factor-beta activated cells». Cytokine Growth Factor Rev. 10 (3–4): 187-99. PMID 10647776. doi:10.1016/S1359-6101(99)00012-X.
- ↑ Wrana JL (1998). «TGF-beta receptors and signalling mechanisms». Mineral and electrolyte metabolism 24 (2–3): 120-30. PMID 9525694. doi:10.1159/000057359.
- ↑ Suazo, José, Santos, José Luis, Jara, Lilian, & Blanco, Rafael. (2008). Assessment of the association between SMAD1 and HHIP gene variation and non-syndromic cleft-lip palate in Chilean case-parent trios Genetics and Molecular Biology, 31(3), 639-642. Accesado el 18 de diciembre de 2015.
- ↑ Moustakas A, Souchelnytskyi S, Heldin CH (2001). «Smad regulation in TGF-beta signal transduction». J. Cell. Sci. 114 (Pt 24): 4359-69. PMID 11792802.
- ↑ Bai S, Shi X, Yang X, Cao X (marzo de 2000). «Smad6 as a transcriptional corepressor». J. Biol. Chem. 275 (12): 8267-70. PMID 10722652. doi:10.1074/jbc.275.12.8267.
- ↑ Kimura N, Matsuo R, Shibuya H, Nakashima K, Taga T (junio de 2000). «BMP2-induced apoptosis is mediated by activation of the TAK1-p38 kinase pathway that is negatively regulated by Smad6». J. Biol. Chem. 275 (23): 17647-52. PMID 10748100. doi:10.1074/jbc.M908622199.
- ↑ Yanagisawa M, Nakashima K, Takeda K, Ochiai W, Takizawa T, Ueno M, Takizawa M, Shibuya H, Taga T (diciembre de 2001). «Inhibition of BMP2-induced, TAK1 kinase-mediated neurite outgrowth by Smad6 and Smad7». Genes Cells 6 (12): 1091-9. PMID 11737269. doi:10.1046/j.1365-2443.2001.00483.x.
- ↑ Topper JN, Cai J, Qiu Y, Anderson KR, Xu YY, Deeds JD, Feeley R, Gimeno CJ, Woolf EA, Tayber O, Mays GG, Sampson BA, Schoen FJ, Gimbrone MA, Falb D (agosto de 1997). «Vascular MADs: two novel MAD-related genes selectively inducible by flow in human vascular endothelium». Proc. Natl. Acad. Sci. U.S.A. 94 (17): 9314-9. PMC 23174. PMID 9256479. doi:10.1073/pnas.94.17.9314.
- ↑ Imoto S, Sugiyama K, Muromoto R, Sato N, Yamamoto T, Matsuda T (septiembre de 2003). «Regulation of transforming growth factor-beta signaling by protein inhibitor of activated STAT, PIASy through Smad3». J. Biol. Chem. 278 (36): 34253-8. PMID 12815042. doi:10.1074/jbc.M304961200.
- ↑ Datta PK, Moses HL (mayo de 2000). «STRAP and Smad7 synergize in the inhibition of transforming growth factor beta signaling». Mol. Cell. Biol. 20 (9): 3157-67. PMC 85610. PMID 10757800. doi:10.1128/MCB.20.9.3157-3167.2000.
 Datos: Q14904336
Datos: Q14904336


 Datos: Q14904336
Datos: Q14904336










