Sitrulina
 | |
 | |
| Nama | |
|---|---|
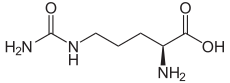
| Nama IUPAC Asid 2-amino-5-(karbamoilamino)pentanoik[1] | |
| Pengecam | |
No. Pendaftaran CAS |
|
Imej model 3D Jmol |
|
| 3DMet |
|
Rujukan Beilstein | 1725417, 1725415 D, 1725416 L |
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.006.145 |
| Nombor EC |
|
Rujukan Gmelin | 774677 L |
IUPHAR/BPS |
|
| KEGG |
|
| MeSH | Citrulline |
PubChem CID |
|
| UNII |
|
CompTox Dashboard (EPA) |
|
InChI
| |
SMILES
| |
| Sifat | |
Formula kimia | C6H13N3O3 |
| Jisim molar | 175.19 g·mol−1 |
| Rupa bentuk | Hablur putih |
| Bau | Tidak berbau |
| log P | −1.373 |
| Keasidan (pKa) | 2.508 |
| Kebesan (pKb) | 11.489 |
| Termokimia | |
| Muatan haba tentu, C | 232.80 J K−1 mol−1 |
| Entropi molar piawai S | 254.4 J K−1 mol−1 |
| Sebatian berkaitan | |
Asid alkanoik berkaitan |
|
Sebatian berkaitan |
|
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
 Y pengesahan (apa yang perlu: Y pengesahan (apa yang perlu:  Y/ Y/ N?) N?) | |
| Rujukan kotak info | |
Sitrulina ialah sebatian organik asid α-amino.[2] Namanya berasal daripada citrullus, perkataan Latin bagi tembikai. Walaupun dinamakan dan dihuraikan oleh pakar gastroenterologi sejak akhir abad ke-19, ia pertama kali diasingkan daripada tembikai pada tahun 1914 oleh penyelidik Jepun, Yotaro Koga dan Ryo Odake,[3][note 1] dan dikaji lebih lanjut oleh Mitsunori Wada dari Universiti Imperial Tokyo pada 1930.[4]
Ia memiliki formula kimia H2NC(O)NH(CH2)3CH(NH2)CO2H. Ia merupakan molekul perantara utama dalam kitaran urea, laluan di mana mamalia mengeluarkan ammonia dengan menukarkannya kepada urea. Sitrulina juga dihasilkan sebagai hasil sampingan daripada enzim pengeluaran nitrik oksida daripada asid amino arginina, dimangkinkan oleh nitrik oksida sintase.ref>"Nos2 - Nitric Oxide Synthase". Uniprot.org. Uniprot Consortium. Dicapai pada 10 February 2015.</ref>
Biosintesis
Sitrulina boleh diperoleh daripada:
- arginina melalui nitrik oksida sintase sebagai hasil sampingan penghasilan nitrik oksida bagi tujuan pengisyaratan
- ornitina melalui pecahan prolina atau glutamina/glutamat
- dimetilarginina asimetri melalui DDAH
Sitrulina diperbuat daripada ornitina dan karbamoil fosfat dalam salah satu tindak balas pusat dalam kitaran urea. Ia juga dihasilkan daripada arginina sebagai hasil sampingan tindak balas yang dimangkin oleh keluarga NOS(NOS; EC 1.14.13.39).[5] Ia juga banyak wujud dalam trikohialin, yakni di kawasan akar dalam dan medula folikel rambut, di mana ia dihasilkan daripada arginina.[6] Arginina mula-mula dioksidakan menjadi N-hidroksil-arginina, dan kemudiannya dioksidakan lagi kepada sitrulina seiring dengan pembebasan nitrik oksida.
Sitrulina juga dihasilkan oleh enterosit usus kecil.[2][7]
Fungsi
Sitrulina ialah molekul perantaraan metabolik dalam kitaran urea, laluan di mana mamalia mengeluarkan ammonia dengan menukarkannya kepada urea. Sitrulina juga dihasilkan sebagai hasil sampingan penghasilan enzim oksida nitrik daripada arginina, dan dimangkinkan oleh nitrik oksida sintase. Dalam spesies yis Saccharomyces cerevisiae, sitrulina ialah perantara metabolisme dalam bahagian sitosol akhir laluan biosintesis arginina.[8]
Beberapa protein mengandungi sitrulina hasil daripada pengubahsuaian pascaterjemahan. Sisa sitrulina ini dihasilkan oleh keluarga enzim yang dipanggil peptidilarginina deiminase (PAD) yang menukarkan arginina kepada sitrulina dalam proses yang dipanggil pensitrulinaan atau penyahiminaan dengan bantuan ion kalsium. Protein yang biasanya mengandungi sisa sitrulina termasuk protein asas mielin (MBP), filagrin dan beberapa protein histon, manakala protein lain seperti fibrin dan vimentin terdedah kepada sitrulina semasa kematian sel dan keradangan tisu.
Sitrulina peredaran ialah biopenanda kefungsian usus.[9][10]
Nota
- ^ Rujukan awal mengeja nama Ryo Odake sebagai Ryo Othake.
Rujukan
- ^ "Citrulline - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information. 16 September 2004. Identification. Dicapai pada 1 May 2012.
- ^ a b Banerjee, Aryamitra (2014-01-01), Gupta, Ramesh C. (penyunting), "Chapter 15 - Gastrointestinal toxicity biomarkers", Biomarkers in Toxicology (dalam bahasa Inggeris), Boston: Academic Press, m/s. 269–277, doi:10.1016/b978-0-12-404630-6.00015-4, ISBN 978-0-12-404630-6, S2CID 88798984, dicapai pada 2020-11-10
- ^ Fragkos, Konstantinos C.; Forbes, Alastair (September 2011). "Was citrulline first a laxative substance? The truth about modern citrulline and its isolation" (PDF). Nihon Ishigaku Zasshi. [Journal of Japanese History of Medicine]. 57 (3): 275–292. ISSN 0549-3323. PMID 22397107. Diarkibkan (PDF) daripada yang asal pada 2022-10-09.
- ^ Fearon, William Robert (1939). "The Carbamido Diacetyl Reaction: A Test For Citrulline". Biochemical Journal. 33 (6): 902–907. doi:10.1042/bj0330902. PMC 1264464. PMID 16746990.
- ^ Cox M, Lehninger AL, Nelson DR (2000). Lehninger principles of biochemistry (ed. 3rd). New York: Worth Publishers. m/s. 449. ISBN 978-1-57259-153-0. Dicapai pada 13 March 2020.
- ^ Rogers, G. E.; Rothnagel, J. A. (1983). "A sensitive assay for the enzyme activity in hair follicles and epidermis that catalyses the peptidyl-arginine-citrulline post-translational modification". Current Problems in Dermatology. 11: 171–184. doi:10.1159/000408673. ISBN 978-3-8055-3752-0. PMID 6653155.
- ^ DeLegge, Mark H. (2019-01-01), Corrigan, Mandy L.; Roberts, Kristen; Steiger, Ezra (penyunting), "Chapter 7 - Enteral Access and Enteral Nutrition in Patients With Short Bowel Syndrome", Adult Short Bowel Syndrome (dalam bahasa Inggeris), Academic Press, m/s. 81–96, doi:10.1016/b978-0-12-814330-8.00007-x, ISBN 978-0-12-814330-8, S2CID 81295089, dicapai pada 2020-11-10
- ^ "Saccharomyces cerevisiae citrulline biosynthesis".
- ^ Fragkos, Konstantinos C.; Forbes, Alastair (2017-10-12). "Citrulline as a marker of intestinal function and absorption in clinical settings: A systematic review and meta-analysis". United European Gastroenterology Journal (dalam bahasa Inggeris). 6 (2): 181–191. doi:10.1177/2050640617737632. PMC 5833233. PMID 29511548.
- ^ Crenn, P.; dll. (2000). "Post-absorptive plasma citrulline concentration is a marker of intestinal failure in short bowel syndrome patients". Gastroenterology. 119 (6): 1496–505. doi:10.1053/gast.2000.20227. PMID 11113071.










