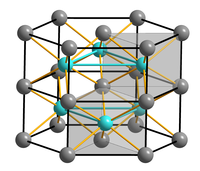
Сульфид кобальта(II)
| Сульфид кобальта(II) | |
|---|---|
| Общие | |
| Систематическое наименование | Сульфид кобальта(II) |
| Традиционные названия | Сернистый кобальт |
| Хим. формула | CoS |
| Рац. формула | CoS |
| Физические свойства | |
| Состояние | зелёные или красновато-бурые кристаллы |
| Молярная масса | 91,00 г/моль |
| Плотность | 5,45 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1100; 1118; 1180 °C |
| Классификация | |
| Рег. номер CAS | 1317-42-6 |
| PubChem | 14832 |
| Рег. номер EINECS | 215-273-3 |
| SMILES | S=[Co] |
| InChI | InChI=1S/Co.S VRRFSFYSLSPWQY-UHFFFAOYSA-N |
| RTECS | GG332500 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

Сульфи́д ко́бальта(II) — бинарное неорганическое соединение, соль металла кобальта и сероводородной кислоты с химической формулой CoS, серые кристаллы, нерастворимые в воде.
Нахождение в природе
В природе встречается минерал джайпурит — β-CoS с различными примесями.
Получение
Сплавлением порошка кобальта и серы:
Осаждением растворимой соли двухвалентного кобальта, например, хлорида кобальта(II) гидросульфидом аммония, при этом образуется α-CoS:
Осаждением растворимой соли двухвалентного кобальта кобальта сероводородом в растворе с уксусной кислотой:
Восстановлением сульфата кобальта углеродом (коксом):
Физические свойства
Сульфид кобальта(II) имеет несколько аллотропных модификаций:
- α-CoS, чёрный аморфный осадок.
- β-CoS, серые кристаллы, гексагональная сингония, пространственная группа P 63/mmc, параметры ячейки a = 0,3385, c = 0,5213 нм, Z = 2.
- γ-CoS, неустойчивая ромбоэдрическая модификация.
В виде порошка пирофорен.
Не растворяется в воде, р ПР = 19,75.
Химические свойства
Разлагается при сильном нагревании:
Реагирует с разбавленными кислотами:
Окисляется горячей концентрированной азотной кислотой:
Во влажном состоянии медленно окисляется кислородом воздуха:
При нагревании окисляется кислородом воздуха:
Применение
Применяется в органическом синтезе в качестве катализатора для гидрирования под давлением органических соединений[1].
Примечания
- ↑ Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1667.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
| H2S | |||||||||||||||||
| Li2S | BeS | B2S3 BS2 B2S5 | CS2 | NH4HS (NH4)2S H8N2MoS4 | O | F | |||||||||||
| Na2S NaHS NaCrS2 | MgS | Al2S3 | SiS SiS2 | P4S3 P4S7 P4S10 | S | Cl | |||||||||||
| K2S KBiS2 KFeS2 KHS K2Pt4S6 KCrS2 | CaS Сa(HS)2 | ScS Sc2S3 | Ti6S Ti16S21 Ti2S TiS Ti8S9 Ti8S10 Ti2S3 TiS2 TiS3 | V3S V5S4 VS V2S3 V5S8 VS2 V2S5 VS4 | CrS Cr5S6 Cr7S8 Cr3S4 Cr2S3 CoCr2S4 KCrS2 NaCrS2 | MnS MnS2 | FeS FeS2 CuFeS2 Fe3S4 Fe2S3 KFeS2 | CoS CoS2 Co9S8 Co3S4 CoCr2S4 Co2S3 CoAsS | Ni2S Ni3S2 Ni6S5 Ni7S6 NiS2 NiS Ni3S4 | Cu2S CuS CuFeS2 CuS2 | ZnS | Ga2S GaS Ga2S3 | GeS GeS2 | As4S4 As4S5 As4S3 As2S3 As2S5 | Se6S2 SeS SeS2 Se2S6 | Br | |
| Rb2S | SrS SrS2 | YS Y5S7 Y2S3 YS2 | Zr9S2 ZrS2 Zr3S2 ZrS Zr2S ZrOS ZrS3 | NbS NbS2 NbS2Br2 NbS2Cl2 NbS3 | Mo2S3 MoS2 MoS3 | Tc2S7 | RuS2 | Rh17S15 Rh2S3 RhS2 | Pd4S Pd3S Pd16S7 Pd2S PdS PdS2 | Ag2S AgS Ag3SbS3 | CdS | In2S InS In6S7 In3S4 In2S3 In3S5 | SnS Sn3S4 Sn2S3 SnS2 | Sb2S3 Sb2S5 | Te | I | |
| Cs2S Cs2S2 Cs2S3 Cs2S5 Cs2S6 | BaS Ba(HS)2 | Hf2S HfS Hf2S3 HfS2 HfS3 | Ta6S Ta2S TaS2 TaS3 | WS2 WS3 | ReS ReS2 Re2S7 | OsS2 OsS4 | IrS Ir2S3 IrS2 IrS3 | PtS K2Pt4S6 Pt2S3 PtS2 | Au2S AuS Au2S3 | Hg2S HgS Hg3S2Cl2 | Tl2S TlS Tl2S3 Tl2S5 | PbS PbS2 | BiS KBiS2 Bi2S3 BiSI BiSCl | PoS | At | ||
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | ||
| ↓ | |||||||||||||||||
| LaS La3S4 La2O2S La2S3 LaS2 | CeS Ce3S4 Ce5S7 Ce2S3 CeS2 | PrS Pr5S7 Pr3S4 Pr2O2S Pr2S3 PrS2 | NdS Nd3S4 Nd2O2S Nd2S3 | Pm | SmS Sm3S4 Sm2S3 | EuS Eu3S4 Eu2O2S Eu2S3 | GdS Gd2S3 GdS2 | Tb | DyS Dy5S7 Dy2S3 DyS2 | HoS Ho5S7 Ho2O2S Ho2S3 | Er5S7 ErS Er2S3 | Tm | YbS Yb3S4 Yb2S3 | LuS Lu2O2S Lu2S3 | |||
| Ac2S3 | US U2S3 US2 U2S5 US3 | PaOS | ThS Th2S3 Th7S12 ThS2 Th2S5 | NpS Np2S3 NpOS Np3S5 NpS3 | PuS Pu2O2S Pu2S3 PuS2 | Am2S3 | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||