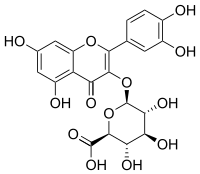
Miquélianine
| Miquélianine | |
 | |
| Identification | |
|---|---|
| Nom UICPA | acide (2S,3S,4S,5R,6S)-6-[2-(3,4-dihydroxyphényl)-5,7-dihydroxy-4-oxochromén-3-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylique |
| Synonymes | Quercétine 3-O-glucuronide |
| No CAS | 22688-79-5 |
| PubChem | 5274585 |
| SMILES | C1=CC(=C(C=C1C2=C(C(=O)C3=C(C=C(C=C3O2)O)O)OC4C(C(C(C(O4)C(=O)O)O)O)O)O)O PubChem, vue 3D |
| Propriétés chimiques | |
| Formule | C21H18O13 |
| Masse molaire[1] | 478,359 8 ± 0,022 g/mol C 52,73 %, H 3,79 %, O 43,48 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
La miquélianine est un composé organique de la famille des flavonols, un sous-groupe de flavonoïdes. C'est plus précisément un hétéroside de flavonol, le 3-O-glucuronide de la quercétine (quercétol). C'est l'un des composés phénoliques présents dans le vin[2], mais également dans certaines espèces de millepertuis[3], comme le millepertuis perforé (Hypericum hirsutum)[4], dans le Lotus sacré (Nelumbo nucifera)[5], ou encore dans les haricots verts[6].
La miquélianine est également un métabolite de la quercétine présent dans le plasma sanguin des rats[7]. Elle présent un effet antioxydant dans le plasma sanguin humain[8]. Des études in vitro ont montré que la miquélianine pouvait atteindre le système nerveux central depuis l'intestin grêle[9].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Miquelianin » (voir la liste des auteurs).
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ A. Ghiselli, M. Nardini, A. Baldi et C. Scaccini, « Antioxidant Activity of Different Phenolic Fractions Separated from an Italian Red Wine », Journal of Agricultural and Food Chemistry, vol. 46, no 2, , p. 361–367 (PMID 10554247, DOI 10.1021/jf970486b)
- ↑ Y. Wei, Q. Xie, W. Dong et Y. Ito, « Separation of epigallocatechin and flavonoids from Hypericum perforatum L. By high-speed counter-current chromatography and preparative high-performance liquid chromatography », Journal of Chromatography A, vol. 1216, no 19, , p. 4313–4318 (PMID 19150073, PMCID 2777726, DOI 10.1016/j.chroma.2008.12.056)
- ↑ G. M. Kitanov, « Miquelianin and other polyphenols from Hypericum hirsutum », Chemistry of Natural Compounds, vol. 24, , p. 119–120 (DOI 10.1007/BF00597593)
- ↑ Y. Kashiwada, A. Aoshima, Y. Ikeshiro, Y. P. Chen, H. Furukawa, M. Itoigawa, T. Fujioka, K. Mihashi, L. M. Cosentino, S. L. Morris-Natschke et K. H. Lee, « Anti-HIV benzylisoquinoline alkaloids and flavonoids from the leaves of Nelumbo nucifera, and structure–activity correlations with related alkaloids », Bioorganic & Medicinal Chemistry, vol. 13, no 2, , p. 443–448 (PMID 15598565, DOI 10.1016/j.bmc.2004.10.020)
- ↑ G. W. Plumb, K. R. Price et G. Williamson, « Antioxidant properties of flavonol glycosides from green beans », Redox Report, vol. 4, no 3, , p. 123–127 (PMID 10496415, DOI 10.1179/135100099101534800)
- ↑ J. H. Moon, T. Tsushida, K. Nakahara et J. Terao, « Identification of quercetin 3-O-β-D-glucuronide as an antioxidative metabolite in rat plasma after oral administration of quercetin », Free Radical Biology and Medicine, vol. 30, no 11, , p. 1274–1285 (PMID 11368925, DOI 10.1016/S0891-5849(01)00522-6)
- ↑ J. Terao, S. Yamaguchi, M. Shirai, M. Miyoshi, J. H. Moon, S. Oshima, T. Inakuma, T. Tsushida et Y. Kato, « Protection by quercetin and quercetin 3-O-β-D-glucuronide of peroxynitrite-induced antioxidant consumption in human plasma low-density lipoprotein », Free Radical Research, vol. 35, no 6, , p. 925–931 (PMID 11811543, DOI 10.1080/10715760100301421)
- ↑ G. Juergenliemk, K. Boje, S. Huewel, C. Lohmann, H. J. Galla et A. Nahrstedt, « In VitroStudies Indicate that Miquelianin (Quercetin 3-O-ß-D-Glucuronopyranoside) is Able to Reach the CNS from the Small Intestine », Planta Medica, vol. 69, no 11, , p. 1013–1017 (PMID 14735439, DOI 10.1055/s-2003-45148)
v · m | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Flavonols |
| ||||||||||||||||
| flavonols O-méthylés |
| ||||||||||||||||
| Flavonols substitués |
| ||||||||||||||||
 Portail de la chimie
Portail de la chimie












