| COL6A2 |
|---|
|
| Ідентифікатори |
|---|
| Символи | COL6A2, PP3610, BTHLM1, UCMD1, collagen type VI alpha 2, collagen type VI alpha 2 chain |
|---|
| Зовнішні ІД | OMIM: 120240 MGI: 88460 HomoloGene: 1392 GeneCards: COL6A2 |
|---|
| |
| Пов'язані генетичні захворювання |
|---|
| Bethlem myopathy, Ullrich congenital muscular dystrophy[1] |
| |
| Реагує на сполуку |
|---|
| ocriplasmin[2] |
| Онтологія гена |
|---|
| Молекулярна функція | • GO:0001948, GO:0016582 protein binding
• extracellular matrix structural constituent conferring tensile strength
|
|---|
| Клітинна компонента | • extracellular vesicle
• Сарколема
• Колаген
• endoplasmic reticulum lumen
• екзосома
• мембрана
• GO:0005578 Позаклітинна матриця
• extracellular region
• міжклітинний простір
• GO:0009327 protein-containing complex
• collagen-containing extracellular matrix
|
|---|
| Біологічний процес | • collagen catabolic process
• protein heterotrimerization
• адгезія клітин
• extracellular matrix organization
• response to glucose
• growth plate cartilage chondrocyte morphogenesis
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|

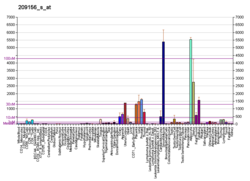 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_001849
NM_058174
NM_058175 |
| |
|---|
| RefSeq (білок) | | NP_001840
NP_478054
NP_478055 |
| |
|---|
| Локус (UCSC) | Хр. 21: 46.1 – 46.13 Mb | Хр. 10: 76.43 – 76.46 Mb |
|---|
| PubMed search | [3] | [4] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
COL6A2 (англ. Collagen type VI alpha 2 chain) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 21-ї хромосоми.[5] Довжина поліпептидного ланцюга білка становить 1 019 амінокислот, а молекулярна маса — 108 579[6].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MLQGTCSVLL | | LWGILGAIQA | | QQQEVISPDT | | TERNNNCPEK | | TDCPIHVYFV |
| LDTSESVTMQ | | SPTDILLFHM | | KQFVPQFISQ | | LQNEFYLDQV | | ALSWRYGGLH |
| FSDQVEVFSP | | PGSDRASFIK | | NLQGISSFRR | | GTFTDCALAN | | MTEQIRQDRS |
| KGTVHFAVVI | | TDGHVTGSPC | | GGIKLQAERA | | REEGIRLFAV | | APNQNLKEQG |
| LRDIASTPHE | | LYRNDYATML | | PDSTEIDQDT | | INRIIKVMKH | | EAYGECYKVS |
| CLEIPGPSGP | | KGYRGQKGAK | | GNMGEPGEPG | | QKGRQGDPGI | | EGPIGFPGPK |
| GVPGFKGEKG | | EFGADGRKGA | | PGLAGKNGTD | | GQKGKLGRIG | | PPGCKGDPGN |
| RGPDGYPGEA | | GSPGERGDQG | | GKGDPGRPGR | | RGPPGEIGAK | | GSKGYQGNSG |
| APGSPGVKGA | | KGGPGPRGPK | | GEPGRRGDPG | | TKGSPGSDGP | | KGEKGDPGPE |
| GPRGLAGEVG | | NKGAKGDRGL | | PGPRGPQGAL | | GEPGKQGSRG | | DPGDAGPRGD |
| SGQPGPKGDP | | GRPGFSYPGP | | RGAPGEKGEP | | GPRGPEGGRG | | DFGLKGEPGR |
| KGEKGEPADP | | GPPGEPGPRG | | PRGVPGPEGE | | PGPPGDPGLT | | ECDVMTYVRE |
| TCGCCDCEKR | | CGALDVVFVI | | DSSESIGYTN | | FTLEKNFVIN | | VVNRLGAIAK |
| DPKSETGTRV | | GVVQYSHEGT | | FEAIQLDDER | | IDSLSSFKEA | | VKNLEWIAGG |
| TWTPSALKFA | | YDRLIKESRR | | QKTRVFAVVI | | TDGRHDPRDD | | DLNLRALCDR |
| DVTVTAIGIG | | DMFHEKHESE | | NLYSIACDKP | | QQVRNMTLFS | | DLVAEKFIDD |
| MEDVLCPDPQ | | IVCPDLPCQT | | ELSVAQCTQR | | PVDIVFLLDG | | SERLGEQNFH |
| KARRFVEQVA | | RRLTLARRDD | | DPLNARVALL | | QFGGPGEQQV | | AFPLSHNLTA |
| IHEALETTQY | | LNSFSHVGAG | | VVHAINAIVR | | SPRGGARRHA | | ELSFVFLTDG |
| VTGNDSLHES | | AHSMRKQNVV | | PTVLALGSDV | | DMDVLTTLSL | | GDRAAVFHEK |
| DYDSLAQPGF | | FDRFIRWIC |
Кодований геном білок за функцією належить до фосфопротеїнів. Задіяний у таких біологічних процесах, як клітинна адгезія, альтернативний сплайсинг. Локалізований у мембрані, позаклітинному матриксі. Також секретований назовні.
Література
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Jander R., Rauterberg J., Glanville R.W. (1983). Further characterization of the three polypeptide chains of bovine and human short-chain collagen (intima collagen). Eur. J. Biochem. 133: 39—46. PMID 6852033 DOI:10.1111/j.1432-1033.1983.tb07427.x
- Nishiyama A., Stallcup W.B. (1993). Expression of NG2 proteoglycan causes retention of type VI collagen on the cell surface. Mol. Biol. Cell. 4: 1097—1108. PMID 8305732 DOI:10.1091/mbc.4.11.1097
- Tillet E., Ruggiero F., Nishiyama A., Stallcup W.B. (1997). The membrane-spanning proteoglycan NG2 binds to collagens V and VI through the central nonglobular domain of its core protein. J. Biol. Chem. 272: 10769—10776. PMID 9099729 DOI:10.1074/jbc.272.16.10769
- Saitta B., Timpl R., Chu M.-L. (1992). Human alpha 2(VI) collagen gene. Heterogeneity at the 5'-untranslated region generated by an alternate exon. J. Biol. Chem. 267: 6188—6196. PMID 1556127
- Saitta B., Stokes D.G., Vissing H., Timpl R., Chu M.-L. (1990). Alternative splicing of the human alpha 2(VI) collagen gene generates multiple mRNA transcripts which predict three protein variants with distinct carboxyl termini. J. Biol. Chem. 265: 6473—6480. PMID 1690728
Примітки
- ↑ Захворювання, генетично пов'язані з COL6A2 переглянути/редагувати посилання на ВікіДаних.
- ↑ Сполуки, які фізично взаємодіють з COL6A2 переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:2212 (англ.) . Архів оригіналу за 10 вересня 2015. Процитовано 12 вересня 2017.
- ↑ UniProt, P12110 (англ.) . Архів оригіналу за 2 вересня 2017. Процитовано 12 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|













